Легочная васкуляризация и вентиляция следуют за разделением бронхиального дерева, что приводит к образованию 10 сегментов в правом легком и 8 сегментов в левом легком. Бронхо-легочные сегменты не являются полностью функционально независимыми. Смежные сегменты имеют общий лимфатический и венозный дренаж, а воздух проходит через границы сегментов по мере необходимости.
Перфузия:
Легочное кровообращение — это система с низким сопротивлением и высокой пропускной способностью.
У взрослых насчитывается около 280 миллионов легочных артериол; у младенцев их значительно меньше. Количество быстро увеличивается на первом году жизни и более постепенно до 8-летнего возраста.
В каждом участке легкого объем кровотока определяется альвеолярным, легочным артериальным, легочным венозным и интерстициальным давлением. Гравитация определяет градиент давления между вершиной и основанием.
В верхних отделах легких альвеолярное давление превышает давление легочной артерии, что приводит к коллапсу капилляров и кровотоку только во время систолических пиков; в базальных отделах, напротив, артериальное давление преобладает над альвеолярным и кровоток непрерывный.
В результате перфузия увеличивается в 3-5 раз от вершины к основанию при ортостатизме.
Вентиляция:
В легких насчитывается 250-300 миллионов альвеол, объединенных в дольки и отделенных друг от друга богатыми сосудистыми альвеолярными перегородками. Вентиляция также имеет градиент давления и увеличивается в 1,5-2 раза от верхушки к основанию.
В случаях вентиляционной обструкции ателектаз предотвращается наличием пор Кона (между смежными альвеолами) и каналов Ламберта (между респираторными бронхиолами и между смежными альвеолярными протоками), которые позволяют воздуху достигать областей ниже обструкции. Однако этот механизм не исправляет альвеолярную гипоксию.
Соотношение вентиляции и перфузии (V/P):
Это очень важный фактор в определении степени альвеолярно-капиллярного газообмена.
В норме соотношение V/P уменьшается от значения 2-3 на вершине до 0,6 у основания, что связано с разным характером вентиляционного и перфузионного градиентов.
Существует ряд гомеостатических механизмов для поддержания адекватного соотношения V/P:
Когда вентиляция какого-либо участка легкого снижается, как при бронхоспазме или хроническом бронхите, перфузия уменьшается, чтобы избежать гипооксигенации крови. В острых ситуациях задействуется механизм артериолярной вазоконстрикции, известный как альвеолярно-капиллярный рефлекс фон Эйлера и Лильестранда; в хронических ситуациях кровь отводится в системную циркуляцию через открытие анастомозов с бронхиальными артериями.
Рефлекторная бронхоконстрикция на гипоперфузированных территориях гораздо менее эффективна и только преходяща.

- Это неинвазивный метод оценки перфузии легких легочными артериями.
- Высокая степень безопасности, относительная простота выполнения и низкая стоимость в сочетании с высокой прогностической способностью делают его визуализирующим исследованием первого выбора при подозрении на тромбоэмболию легочной артерии.
Как это делается?
Макроагрегаты или микросферы альбумина, меченные 99mTc, вводятся внутривенно, вызывая преходящую микроэмболизацию небольшой части легочных артериол после прохождения через правое сердце. Распределение радиоактивных частиц в легких в точности повторяет кровоток в момент введения.
- Положение пациента во время введения радиоиндикатора: — в ортостатическом положении или сидя: базальные области более перфузированы — в клиностатическом положении (положение лежа): задние области более перфузированы
- Глубина дыхания действует:
— поверхностное дыхание: более перфузируется внутренняя область — глубокое дыхание: более перфузируется периферическая область.
Какую информацию он предоставляет?
- С помощью изображений, хроматические изменения которых пропорциональны радиоактивности, перфузионная сцинтиграфия легких обеспечивает визуальное представление регионального распределения легочного кровотока во время введения радиофармпрепарата.
Больно ли это?
- Тест не имеет значительных побочных эффектов и хорошо переносится даже пациентами с тяжелыми легочными или сердечными заболеваниями.
- Процедура включает простую внутривенную инъекцию; количество вводимых частиц, которое зависит от веса, очень мало по сравнению с количеством легочных капилляров; микроэмболизация затрагивает менее 1% легочных капилляров, является транзиторной и проходит в течение нескольких часов.
- Микроэмболизация происходит при первом прохождении через легочное русло, и при отсутствии значительного шунта dx-sn частицы не достигают системной циркуляции.
- Наличие шунта dx-sn не является абсолютным противопоказанием, поэтому исследование, после соответствующего снижения дозы частиц, также проводится для изучения легочной перфузии у пациентов со сложными врожденными пороками сердца, даже у детей, или для оценки степени внутрилегочного шунта у пациентов с заболеваниями печени.
- Доза радиации, поглощенная легкими, низкая
- Доза радиации, поглощенная гонадами и всем телом, очень мала
99m Tc-MAA :
Дозы радиации, поглощенные пациентом весом 70 кг
| Орган | мГр/мБк | рад/мКи |
|---|---|---|
| Легкие | 0.040 | 0.15 |
| Костный мозг | 0,003 | 0,01 |
| Гонады | 0.003 | 0.01 |
| Все тело | 0.003 | 0.01 |
Для чего он нужен?
- Оценка подозрения на тромбоэмболию легочной артерии.
- Проверка эффективности тромболитико-антикоагулянтной терапии.
- Изучение перфузионных изменений, вторичных по отношению к легочным патологиям, таким как эмфизема, хронический бронхит, астма, воспалительные заболевания и новообразования.
- Исследование изменений легочной перфузии, вторичных по отношению к заболеваниям сердца.
- Прогнозирование гемодинамической переносимости операции иссечения легких .
- Исследование правостороннего шунта (первичное или вторичное по отношению к заболеванию печени).

- Это неинвазивное исследование, которое позволяет посредством вдыхания инертных газов или аэрозолей оценить вентиляцию в различных отделах легких.
- Когда показанием является тромбоэмболия легочной артерии, она связана с перфузионным исследованием.
Как это делается?
- Используются инертные газы, такие как 133 Xe, 127 Xe или 81m Kr, псевдогазы, такие как 99m Tc-Technegas (ультратонкие частицы углерода), или аэрозоли, обычно 99mTc-DTPA (диэтилентриамин-пентауксусная кислота) или 99mTc-коллоидный сульфид, которые вдыхаются пациентом для наблюдения за их распределением в легких.
- Методика выполнения и, частично, получаемая информация, могут варьироваться в зависимости от используемых радиофармацевтических препаратов.
Для чего он используется?
- Дифференциальная диагностика между легочной эмболией и другими патологиями, которые могут изменять легочную перфузию, когда перфузионная сцинтиграфия не показывает достаточной специфичности, особенно у пациентов с отклонениями на рентгене.
- Исследование легочной вентиляции при обструктивных заболеваниях бронхов, таких как хроническая обструктивная болезнь легких, новообразования бронхов или др.
- Исследование легочной проницаемости (с субмикронным аэрозолем 99mTc-DTPA).
- Исследование мукоцилиарного клиренса (с мечеными коллоидами)
Больно ли это?
- Вентиляционное исследование полностью исключает риск для пациента. Для его выполнения пациенту достаточно дышать в маску.
- В зависимости от химической и физической природы радиофармацевтические препараты выводятся из организма путем выдоха, почечной экскреции или слизистого транспорта в желудочно-кишечный тракт.
- Доза радиации, поглощенная легкими, низкая
- Доза радиации, поглощенная гонадами и всем телом, очень мала
133 Ксенон :
Дозы радиации, поглощенные пациентом весом 70 кг
| Орган | мГр/мБк | рад/мКи |
|---|---|---|
| Легкие | 0.0018 | 0.007 |
| Костный мозг | 0.0002 | 0.001 |
| Гонады | 0.0002 | 0.001 |
| Все тело | 0.0002 | 0.001 |

Перфузорные исследования
Макроагрегаты альбумина (МАА)
- Препараты для термической денатурации человеческого альбумина и конъюгатов 99mTc
- Размер: 90% от 5-90 мкм, большинство от 10-40 мкм.
- Биологический период полураспада от 2 до 9 часов в зависимости от размера; после деградации и уменьшения размера они проходят через легочный фильтр и попадают в системную циркуляцию, откуда удаляются ретикуло-эндотелиальной системой селезенки и печени.
Микросферы из человеческого альбумина (HAM)
- При встряхивании сыворотки человеческого альбумина в горячем растительном масле образуются сферические частицы, которые затем фильтруются через отверстия в мембране для определения их размера. Именно поэтому они демонстрируют меньшую вариабельность диаметра, чем MAA. Они также конъюгированы с 99mTc.
- Размер: между 10-45 мкм.
- Однако по сравнению с МАА они имеют некоторые недостатки, такие как более длительный средний биологический период полураспада (7 часов), меньшая стабильность связывания 99mTc и большее, хотя все еще очень небольшое, число зарегистрированных аллергических реакций.
Исследования вентиляторов
1) Благородные газы
133 Ксенон
- Период полураспада: 5,3 дня
- Испускает гамма-излучение с энергией 80 кэВ и ß-излучение с энергией 346 кэВ.
- Позволяет исследовать легочную вентиляцию путем последовательного анализа фаз:
- Умывание : глубокий вдох и задержка дыхания примерно на 15 секунд.
- Баланс : нормальное дыхание с Xe в замкнутом контуре.
- Промывка : Нормальное дыхание окружающим воздухом с выдыханием Xe в закрытой системе.
Этот метод позволяет как измерить распределение вентиляции в различных отделах легких, так и получить кривые накопления и элиминации, полезные при изучении обструктивных заболеваний легких. В случае подозрения на легочную эмболию, Xe-133 имеет тот недостаток, что его необходимо использовать до перфузионного исследования.
Благодаря своей выраженной липофильности, Xe пересекает альвеолярно-капиллярный барьер и достигает системной циркуляции в значительной степени, накапливаясь в жировой ткани.
127 Ксенон
- Период полураспада: 36,4 дня
- Испускает только гамма-излучение с энергией 202, 172 и 375 кэВ
- Дороже и сложнее в приобретении, чем 133Xe
- Позволяет, в дополнение к тому, что описано для 133Xe, получать изображения вентиляции после изображений перфузии, в наиболее подходящих проекциях, чтобы показать дефекты перфузии.
81м Криптон
- Период полураспада:13 секунд
- Испускает только гамма-излучение с энергией 190 кэВ.
- Дорого и трудно хранить, должен производиться рубидий-криптоновым генератором (период полураспада 4,7 ч).
- Пик энергии, благоприятный для визуализации с помощью гамма-камеры и достаточно удаленный от пика энергии 99mTc (140 кэВ), позволяет одновременно получать изображения перфузии и вентиляции в различных проекциях.
- Очень короткий период полураспада, из-за которого в плохо или невентилируемых областях активность снижена или отсутствует, поскольку Kr-81m распадается, не достигнув их, позволяет получать только равновесные изображения.
2) Аэрозоли
Распыляемые частицы, которые могут быть маркированы 99m технецием, 111 индием, 113m индием или другими. Они сильно различаются по размеру (0,5-5 мкм) и оседают вдоль дыхательных путей в зависимости от их размера и скорости вдыхаемого воздуха.
Более крупные частицы (2-5 мкм) откладываются центрально над задней частью гортани и трахеи; только более мелкие, однородные частицы (субмикронные или менее 2 мкм) откладываются дистальнее альвеол.
Они имеют преимущество перед газами в том, что они более доступны и просты в использовании.
99m Tc-DTPA (диэтилен-триамин-пентауксусная кислота)
- Аэрозоли однородных субмикронных частиц, обычно размером менее 2 мкм
- Покидает легкие путем альвеолярно-капиллярного транспорта
- Биологический период полураспада у нормальных людей составляет приблизительно 50 минут и снижается у людей с заболеваниями, которые нарушают легочный интерстиций
- Он удаляется из системной циркуляции главным образом путем гломерулярной фильтрации.
99m Tc-сульфид коллоидный
- Многие различные коллоидные вещества использовались в прошлом для исследований легочной вентиляции
- Размер частиц обычно составляет от 2 мкм до 5 мкм
- Они устраняются мукоцилиарной системой
- Они могут использоваться для исследования мукоцилиарной функции.
3) Pseudogas
Технегас
- Аэрозоль ультратонких частиц углерода (диаметром 4-50 нм), меченных 99mTc.
- Медленно выводится из легких (биологический период полураспада от нескольких часов до нескольких дней), что позволяет проводить томографические исследования
- Элиминация происходит в основном через мукоцилиарную и лимфатическую системы
Пертехнегас
- Аэрозоль ультратонких дисперсных частиц пертенектата (диаметр 25 нм)
- Имеет биологический период полураспада около 10 минут и выводится альвеолярно-капиллярным транспортом
- Получаемые кривые «активность-время» свидетельствуют о легочном интерстициальном нарушении и изменяются у курильщиков или пациентов с оппортунистическими легочными инфекциями.

Масштаб проблемы
Патофизиология
- При острой артериальной обструкции вентиляция вовлеченной территории все еще сохраняется.
- Таким образом, существует несоответствие (» mismatch «) между обнаружением гипоперфузии одного или нескольких участков легких и нормальной вентиляцией этих же участков. Однако в случае обструктивных заболеваний гипоперфузированные участки также подвергаются гиповентиляции (» match «) из-за рефлекторной вазоконстрикции, вызванной снижением давления кислорода в альвеолярном воздухе.
Инструменты диагностики
Интерпретация
- Перфузионная сцинтиграфия имеет очень высокую отрицательную предсказательную способность , и если она нормальная, диагноз эмболии можно практически исключить.
- Патологическая перфузионная сцинтиграфия, напротив, может быть обусловлена любой ситуацией, вызывающей снижение перфузии легких. Это делает перфузионную сцинтиграфию легких очень чувствительной, но сама по себе не очень специфичной. Для правильной интерпретации результаты перфузии должны быть соотнесены с рентгенограммой грудной клетки и, возможно, с вентиляционной сцинтиграфией.
- В случае легочной эмболии наблюдается дискордантность (» mismatch «) между перфузионной и вентиляционной картинами: наблюдается одна или несколько субсегментарных, сегментарных или лобарных областей гипоперфузии, которые вентилируются.
| ПРИМЕР
НЕСООТВЕТСТВИЕ |
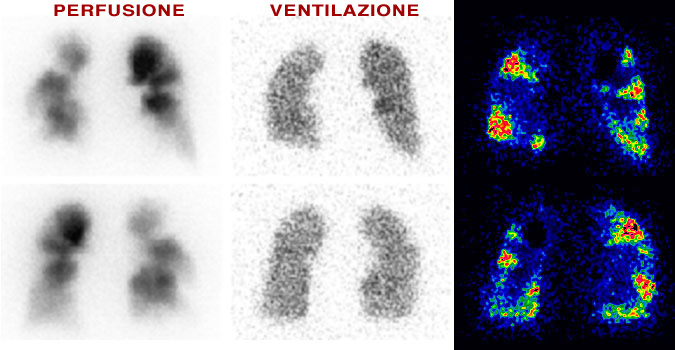 |
|||||||||
|---|---|---|---|---|---|---|---|---|---|---|
- В случае обструктивной патологии наблюдается соответствие (» match «) между перфузионной и вентиляционной картиной: гипоперфузированные участки гиповентилируются.
- Диагноз ВП на основании рентгенографии грудной клетки и сцинтиграфии может быть поставлен только с точки зрения вероятности. Диагностическая стратегия направлена на стратификацию пациентов на основе фактической вероятности наличия эмболии, с целью принятия решения о том, следует ли немедленно приступить к лечению, провести ангиографию или подождать клинического развития.
- Были предложены различные критерии для интерпретации сцинтиграфической картины, основанные на количестве и размере дефектов на сцинтиграфии в сравнении с результатами рентгенографии грудной клетки, с целью получения значения вероятности путем максимального устранения субъективной вариабельности интерпретации. Критерии PIOPED » (Проспективное исследование диагностики легочной эмболии): — высокая вероятность
- Не менее 2 обширных (>75% сегмента) и «несовпадающих» дефектов перфузии без соответствующих отклонений на рентгенограмме грудной клетки.
- 1 обширный и не менее 2 умеренных дефектов перфузии (25-75% сегмента), без соответствующих дефектов вентиляции или отклонений на рентгенограмме грудной клетки.
Уменьшение дефектов перфузии и не менее 4 в «несовпадении», без соответствующих отклонений на рентгенограмме грудной клетки.
— Промежуточная вероятность
- Соответствие в базальной области «совпадающего» дефекта вентиляции и перфузии и паренхимального помутнения на рентгенограмме.
- 1 умеренный «совпадающий» дефект перфузии и вентиляции, без соответствующих отклонений на рентгенограмме грудной клетки
- Перфузия, дефект согласования вентиляции с небольшим плевральным выпотом
- Затрудняюсь классифицировать в других категориях.
— Низкая вероятность
- Множественные «совпадающие» дефекты перфузии и вентиляции, независимо от размера, при отсутствии отклонений на RX.
- Совпадение дефектов вентиляции и перфузии в средней или верхней области и помутнение легких на рентгенограмме.
- Дефекты перфузии и вентиляции при переписке с обширным плевральным выпотом.
- Любой дефект перфузии, соответствующий грубым аномалиям на рентгенограмме.
- Дефекты, окруженные нормально перфузируемыми участками (знак полоски).
- Более 3 маленьких (
- Однако степень клинического подозрения на эмболию перед сцинтиграфией имеет большое значение. Клиническая картина, рассматриваемая вместе с результатом сцинтиграфии, позволяет оценить фактический уровень вероятности того, что у пациента эмболия.
- В целом, пациенты, у которых оценивается высокая вероятность эмболии, должны получать специальное лечение, тогда как пациенты, у которых оценивается промежуточная вероятность, могут нуждаться в ангиографической оценке. У большинства пациентов с низкой вероятностью эмболии предпочтительнее дождаться клинической эволюции или пересмотреть диагностическое подозрение.
