
ПРОФИЛАКТИКА
«Дыхание — это жизнь: измерение дыхания улучшает жизнь»

ПРОФИЛАКТИКА
«Дыхание — это жизнь: измерение дыхания улучшает жизнь»

ПРОФИЛАКТИКА
«Дыхание — это жизнь: измерение дыхания улучшает жизнь»

ПРОФИЛАКТИКА
«Дыхание — это жизнь: измерение дыхания улучшает жизнь»
ДИАГНОЗ БРОНХИАЛЬНАЯ АСТМА
ИСТОРИЯ БОЛЕЗНИ
Правильный сбор анамнестической информации с помощью серии точных вопросов, таких как приведенные ниже, позволяет заподозрить астму примерно у 60% пациентов.
- Случались ли у вас приступы затрудненного дыхания в состоянии покоя, днем и/или ночью, или после физической нагрузки?
- Слышали ли вы когда-нибудь свист или шипение при дыхании, в состоянии покоя днем и/или ночью, или после физической нагрузки?
- Был ли у вас когда-нибудь ноющий кашель, особенно ночью или после физической нагрузки?
- Если у вас была простуда, замечали ли вы, что она легко переходит в бронхит или требует более 10 дней для выздоровления?
- Принимали ли вы нестероидные противовоспалительные препараты или бета-блокаторы?
- Возникает ли затрудненное дыхание преимущественно во время или после еды, ночью или в положении лежа?
- Когда много смога или вы находитесь в период наибольшей концентрации пыльцы, было ли вам когда-нибудь трудно дышать или вы ощущали свист или шипение при этом?
- Было ли у вас когда-нибудь затрудненное дыхание и/или сухой кашель при вдыхании тяжелых ароматов?
- Было ли у вас когда-нибудь ощущение, что жидкость или что-то попадает через нос в горло, с охриплостью, раздражением горла?
- Испытывали ли вы когда-нибудь жжение в груди, кислотную регургитацию или чрезмерное расширение желудка с частой отрыжкой или тошнотой?
- Проходят ли ваши симптомы полностью после лечения противоастматическими препаратами?
Симптомы, о которых чаще всего сообщают больные астмой, — это ощущение затрудненного дыхания и стеснения в груди, хрипы и кашель. Эти симптомы обычно выражены по-разному, хотя в редких случаях они могут встречаться по отдельности. Например, у пациентов с кашлем как проявлением астмы упорный кашель может появляться сам по себе или предшествовать или вызывать эпизод бронхоспазма.
У больного астмой кашель обычно сухой, но когда он возникает в конце астматического криза, то сопровождается выделением небольшого количества вязких, жемчужно-желтых выделений, что приводит к ощущению заметного улучшения дыхательных возможностей. Также у пациента-астматика возможно характерное отхаркивание небольших округлых образований, повторяющих диаметр дыхательных путей, в которых они образовались.
Симптомы возникают в пароксизмальной форме, независимо от того, вызываются ли они различными неспецифическими стимулами, такими как раздражающие пары или газы, холодный воздух, гипервентиляция, вызванная физической нагрузкой, или смех, или специфическими стимулами, как при аллергической или профессиональной астме.
Симптомы также могут возникать или быть более выраженными в определенное время года, что указывает на возможную роль воздействия сезонных аллергенов.
При сборе симптомов частота (ежедневно, еженедельно или ежемесячно), ритм день-ночь и интенсивность важны для определения степени тяжести астмы, учитывая, однако, что некоторые больные астмой плохо воспринимают симптомы и склонны недооценивать как частоту, так и интенсивность астматических проявлений.
История болезни должна также включать такую информацию, как семейная история аллергических или легочных заболеваний, личная история атопических заболеваний (крауроз, экзема, крапивница, ринит, пищевая непереносимость), наличие или отсутствие привычки к курению, профессиональная деятельность.
ОБЪЕКТИВНЫЙ ЭКЗАМЕН
Объективное обследование может быть полностью отрицательным у пациентов с легкой интермиттирующей астмой или когда субъект наблюдается вне респираторного криза. Только периодическое глубокое дыхание или гипервентиляция вызывают приступы сухого кашля.
У пациентов с постоянной тяжелой астмой средней степени тяжести при аускультации грудной клетки можно обнаружить непрерывные шумы, обычно высокого тона (шипение), преимущественно экспираторные, особенно если пациента заставляют выдыхать.
У пациентов с хронической астмой могут наблюдаться признаки обструкции и хронической гиперинфляции (изменения конформации грудной клетки, гиперфонезис сплетений), возможно, связанные с прерывистыми низкочастотными дыхательными шумами (рончи), более характерными для ХОБЛ (хронической обструктивной болезни легких).
У пациентов с тяжелой астмой наблюдается сильная одышка с затруднением речи, тахикардия, использование вспомогательных дыхательных мышц, втягивание межреберных мышц и иногда цианоз. У таких пациентов дыхательные звуки часто могут отсутствовать (дыхательная тишина).
ПОДТВЕРЖДЕНИЕ ДИАГНОСТИЧЕСКОГО ПОДОЗРЕНИЯ
Спирометрия, либо в исходном состоянии, либо после введения одной дозы бронхолитика или после короткого курса антиастматической терапии, мониторинг PEF и тест неспецифической бронхостимуляции являются необходимыми тестами для установления наличия бронхиальной астмы, поскольку именно они могут продемонстрировать наличие переменной бронхоконстрикции, часто обратимой спонтанно или после медикаментозного лечения, и повышенной бронхиальной реактивности
Базовая спирометрия и после бронхолитика
Как правило, у пациентов с умеренной и тяжелой астмой тесты дыхательной функции демонстрируют наличие обструкции дыхательных путей. У этих пациентов обнаружение обратимости бронхиальной обструкции, рассматриваемой как увеличение объема форсированного выдоха за 1 секунду (FEV1) на 12% от исходного уровня и более чем на 200 мл в абсолютном значении после приема 400 мкг сальбутамола, считается достаточным для подтверждения диагностического подозрения на бронхиальную астму.
Типичные кривые спирометрии до и после бронходилатации
- Левая кривая «объем-время»
- Правый поток-объем: до бронходилатации FEV1 равен 2,71 L, после бронходилатации FEV1 3,07 L (увеличение на 13%)
У пациентов с обструкцией дыхательных путей, которые не реагируют остро на бронхолитики, можно оценить увеличение FEV1 после 2-4 недель лечения бронхолитиками и ингаляционными кортикостероидами в высоких дозах.
Исходный уровень и после бронхоконстрикторной спирометрии
Большинство пациентов с легкой интермиттирующей затихающей астмой имеют нормальные показатели функции дыхания, и назначение препарата бронхолитического действия короткого действия не приводит к значительным изменениям исходных функциональных параметров.
В этих случаях фундаментальный инструментальный тест, позволяющий понять, имеет ли кашель астматическое происхождение, представлен измерением гиперреактивности бронхов.
Бронхиальная гиперреактивность характеризуется бронхостриктивной реакцией дыхательных путей на различные неспецифические (физические, химические, фармакологические) или специфические (аллергены, наркотики) бронхоконстрикторные стимулы, которая выражена гораздо сильнее, чем у нездоровых людей. Неспецифические стимулы вызывают бронхоконстрикцию у большинства астматических пациентов независимо от этиологии заболевания; некоторые из них более чувствительны, но менее специфичны (например, холинергические фармакологические стимулы), другие менее чувствительны, но более специфичны (например, физические стимулы) и, вероятно, определяют наиболее тяжелую категорию пациентов.
В клинической практике тест проводится путем вдыхания возрастающих концентраций (или доз) неспецифического бронхоконстрикторного агента (обычно метахолина) через небулайзер; ингаляция продолжается до достижения максимальной дозируемой концентрации или до снижения FEV1 на 20% или более от исходного уровня.
Результаты выражаются как провокационная концентрация (или доза) (PC20FEV1 или PD20FEV1) в мг/мл (или мкг) метахолина; значение получено из кривой «доза-ответ», построенной путем нанесения концентрации метахолина на абсциссы и процентного снижения FEV1 от исходного уровня на ординаты
Кривые «доза-ответ» на метахолин (бронхоконстриктор)
- Слева: кривая «доза-ответ» для метахолина у нормального человека
- Справа: субъект с астмой
В клинической практике тест считается отрицательным, если PC20FEV1 больше 8 мг/мл (или больше примерно 800-1000 мкг в случае PD20FEV1). Бронхиальная гиперреактивность присутствует у большинства пациентов с астмой, поэтому отрицательный тест на бронхостимуляцию метахолином делает диагноз бронхиальной астмы маловероятным. Действительно, исследования показали, что отрицательная прогностическая ценность теста на бронхостимуляцию очень высока (85-95%); напротив, положительная прогностическая ценность колеблется от 60% до 82%. Это связано с тем, что гиперреактивность бронхов присутствует не только у астматиков, но и может быть вызвана другими заболеваниями, такими как вирусные инфекции верхних дыхательных путей, муковисцидоз, гастроэзофагеальная рефлюксная болезнь и хроническая обструктивная болезнь легких.
Мониторинг пикового экспираторного потока (ПЭФ) ПЭФ — это наибольший экспираторный поток, полученный во время форсированного экспираторного маневра, выполненного сразу после максимального вдоха при полной емкости легких
ПЭФ-метры являются простыми, но не очень чувствительными инструментами для демонстрации наличия бронхиальной обструкции, и их использование не рекомендуется для диагностики астмы: они могут использоваться в качестве инструментов мониторинга у пациентов, у которых спирометрическое исследование не может повторяться через регулярные промежутки времени.
Периодический домашний мониторинг PEF иногда полезен для пациентов, чтобы быть в курсе признаков функционального ухудшения.
В идеале, PEF следует измерять дважды в день: утром, когда показатели самые низкие, и вечером, когда показатели обычно самые высокие.
Дополнительные измерения рекомендуются в случае появления астматических симптомов, чтобы оценить важность конкретных триггеров (аллергенов или профессиональных воздействий). Мониторинг PEF обеспечивает простую оценку вариабельности дыхательной функции. Ежедневная вариабельность PEF более 20% или улучшение PEF не менее чем на 15% после ингаляции бронхолитика или после курса стероидной терапии считается признаком астмы.
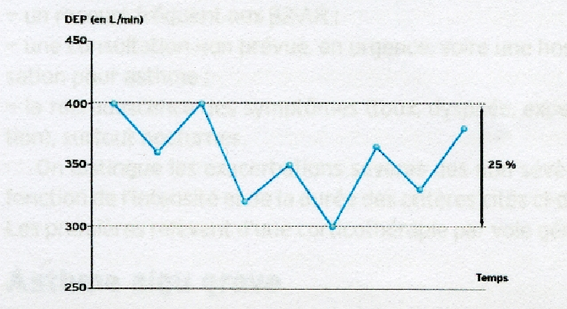
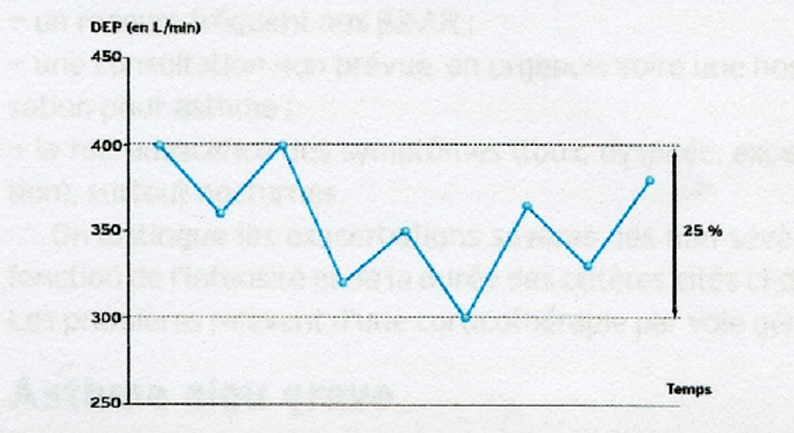
Простой метод расчета вариабельности PEF у субъекта с несколькими измерениями в течение двух недель показан на рисунке ниже:
Вариабельность в % рассчитывается следующим образом :
400 — 300 = 100
100: 400 = 0,25 = 25 %
В этих случаях может быть полезно рассчитать вариабельность с учетом измерений PEF, полученных после действия бронхолитика.
В этих случаях может быть полезно рассчитать вариабельность, учитывая измерения PEF, полученные после действия бронхолитика.
Длительный мониторинг PEF может быть полезен для диагностики, а также для оценки эффективности терапии.
Оптимальная продолжительность мониторинга PEF составляет около 2 недель, возможно, его следует повторять в разное время в течение года.
Как правило, более длительные периоды мониторинга PEF малопригодны из-за отсутствия приверженности пациентов, но могут быть показаны пациентам с тяжелой астмой или плохим восприятием симптомов. Хотя в литературе имеются прогнозируемые значения PEF, из-за большой межиндивидуальной вариабельности рекомендуется использовать индивидуальные прогнозируемые значения, полученные путем мониторинга PEF, когда пациент находится в стабильной фазе заболевания и получает максимальную лекарственную терапию. Определенный таким образом так называемый личный лучший PEF должен рассматриваться как эталон абсолютной величины измерения и оценки вариабельности суточного потока.
Рентген грудной клетки
При астме целью проведения рентгенографии грудной клетки является исключение других диагнозов, таких как наличие бронхоэктазов, ХОБЛ или муковисцидоза, поскольку у большинства больных астмой эта рентгенограмма нормальная.
ДРУГИЕ РАССЛЕДОВАНИЯ
Во многих случаях диагноз бронхиальной астмы может быть легко поставлен на основании вышеуказанных диагностических исследований (базальная спирометрия и после бронходилататора, мониторинг пикового экспираторного потока, бронхиальный провокационный тест с метахолином): как правило, это наиболее типичные пациенты (молодые, некурящие, с аллергическим компонентом), и в этих случаях может не потребоваться проведение других функциональных исследований, кроме рентгенографии грудной клетки для исключения других патологий.
В клинически более сложных и трудных случаях, с вероятностью наложения на другие хронические обструктивные заболевания легких (хронический бронхит и эмфизема) и у лиц с менее типичной клинической картиной (пожилые, курильщики, лица с признаками хронического риносинусита, или гастро-эзофагеального рефлюкса, или аллергического профессионального воздействия, или исследования степени воспаления легких и т.д.) целесообразно прибегнуть к дополнительным исследованиям.), необходимо провести дополнительные исследования в различных соответствующих областях специализации: полная спирометрия, диффузия СО легких, КТ грудной клетки, исследование гиперреактивности бронхов на нефармакологические стимулы или на специфические аллергенные стимулы, исследование индуцированной мокроты, бронхоскопия с бронхоальвеолярным лаважем (БАЛ), биопсия бронхов, измерение оксида азота в выдыхаемом воздухе, КТ околоносовых пазух, pHманометрия пищевода и гастроскопия.
ГЕМАТОХИМИЧЕСКИЕ ИССЛЕДОВАНИЯ
Эозинофилия крови, хотя и не специфична для астмы или ринита и присутствует только у меньшинства людей с активной астмой, может присутствовать как при аллергических, так и неаллергических формах астмы. Самые высокие уровни эозинофилии обнаруживаются при формах внутренней бронхиальной астмы, связанной с полипозом носа; в целом, однако, процент эозинофилов в циркулирующей крови составляет менее 15-20%; более высокие значения должны вызывать подозрение на другие заболевания (связанные с астмой, такие как синдром Чурга-Штрауса и другие).
Анализ общего IgE в сыворотке крови полезен только по двум причинам:
- , чтобы помочь определить статус атопии как фактор риска развития астмы и ринита;
- для установления дозы препарата Anti-IgE (омализумаб) для использования в небольшой группе пациентов с неконтролируемой тяжелой астмой, аллергией на многолетние аллергены.
